ਭਾਰਤ ਨੇ ਬਣਾਈ ਦੇਸ਼ ਦੀ ਪਹਿਲੀ ਦੇਸੀ ਮਲੇਰੀਆ ਵੈਕਸੀਨ
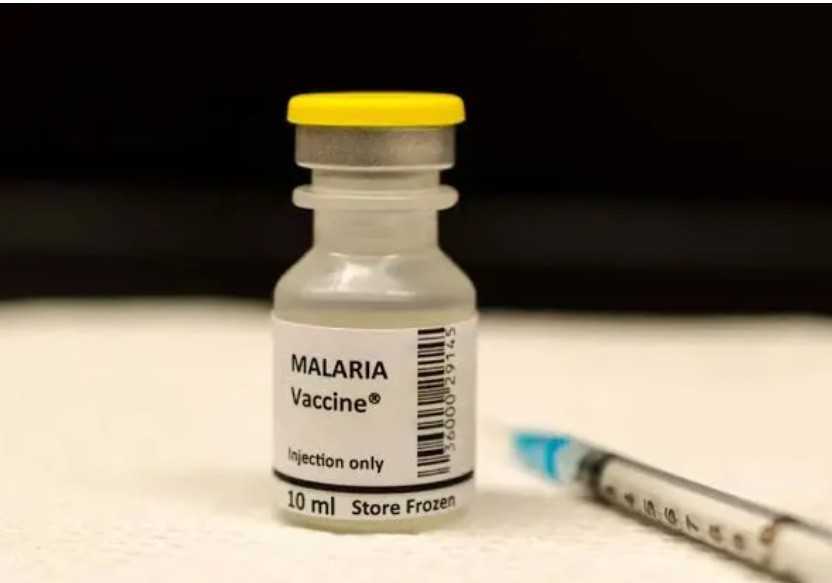

ਨਵੀਂ ਦਿੱਲੀ, 21 ਜੁਲਾਈ (ਨਿਊਜ਼ ਟਾਊਨ ਨੈਟਵਰਕ) : ਭਾਰਤ ਨੇ ਮਲੇਰੀਆ ਵਿਰੁਧ ਇਕ ਵੱਡੀ ਵਿਗਿਆਨਕ ਸਫਲਤਾ ਪ੍ਰਾਪਤ ਕੀਤੀ ਹੈ। ਦੇਸ਼ ਨੇ ਆਪਣਾ ਪਹਿਲਾ ਸਵਦੇਸ਼ੀ ਮਲੇਰੀਆ ਟੀਕਾ ਵਿਕਸਤ ਕਰ ਲਿਆ ਹੈ, ਜਿਸਨੂੰ ਪਲਾਜ਼ਮੋਡੀਅਮ ਫਾਲਸੀਪੈਰਮ ਪਰਜੀਵੀ ਵਿਰੁਧ ਬੇਹਦ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ। ਇਹ ਟੀਕਾ ਨਾ ਸਿਰਫ ਲਾਗ ਨੂੰ ਰੋਕਣ ਵਿਚ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਹੈ, ਬਲਕਿ ਇਸਦੇ ਫੈਲਣ ਨੂੰ ਰੋਕਣ ਦੇ ਵੀ ਸਮਰੱਥ ਹੈ। ਇਹ ਟੀਕਾ ਆਈਸੀਐਮਆਰ ਦੇ ਭੁਵਨੇਸ਼ਵਰ ਸਥਿਤ ਖੇਤਰੀ ਮੈਡੀਕਲ ਖੋਜ ਕੇਂਦਰ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ ਅਤੇ ਇਸਨੂੰ ‘ਐਡਵੈਕਸਫਾਲਸੀ’ (ਐਡਫਾਲਸੀਵੈਕਸ) ਨਾਮ ਦਿਤਾ ਗਿਆ ਹੈ। ਇੰਡੀਅਨ ਕੌਂਸਲ ਆਫ਼ ਮੈਡੀਕਲ ਰਿਸਰਚ (ਆਈਸੀਐਮਆਰ) ਨੇ ਹੁਣ ਇਸ ਟੀਕੇ ਦੇ ਵਪਾਰਕ ਉਤਪਾਦਨ ਲਈ ਤਕਨਾਲੋਜੀ ਟ੍ਰਾਂਸਫਰ ਲਈ ਕੰਪਨੀਆਂ ਅਤੇ ਨਿਰਮਾਤਾਵਾਂ ਤੋਂ ਅਰਜ਼ੀਆਂ ਮੰਗੀਆਂ ਹਨ। ਇਸਦੇ ਲਈ ਦਿਲਚਸਪੀ ਰੱਖਣ ਵਾਲੀਆਂ ਧਿਰਾਂ ਤੋਂ ‘ਐਕਸਪ੍ਰੈਸ਼ਨ ਆਫ਼ ਇੰਟਰਸਟ’ (ਈਓਆਈ) ਮੰਗਿਆ ਗਿਆ ਹੈ।
ਇਸ ਟੀਕੇ ਦੀਆਂ ਵਿਸ਼ੇਸ਼ਤਾ ਦੇ ਮੱਦੇਨਜ਼ਰ ਜਦੋਂ ਪਰਜੀਵੀ ਖੂਨ ਦੇ ਪ੍ਰਵਾਹ ਵਿਚ ਦਾਖਲ ਹੁੰਦਾ ਹੈ ਤਾਂ ਇਹ ਟੀਕਾ ਮਲੇਰੀਆ ਦੇ ਸ਼ੁਰੂਆਤੀ ਪੜਾਵਾਂ ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦਾ ਹੈ। ਇਸਨੂੰ ਲੈਕਟੋਕੋਕਸ ਲੈਕਟਿਸ ਨਾਮਕ ਬੈਕਟੀਰੀਆ ਦੀ ਮਦਦ ਨਾਲ ਤਿਆਰ ਕੀਤਾ ਗਿਆ ਹੈ, ਜੋ ਆਮ ਤੌਰ ‘ਤੇ ਦਹੀਂ ਅਤੇ ਪਨੀਰ ਵਰਗੀਆਂ ਚੀਜ਼ਾਂ ਵਿਚ ਪਾਇਆ ਜਾਂਦਾ ਹੈ। ਇਸ ਟੀਕੇ ਨੂੰ ਵਿਕਸਤ ਕਰਨ ਲਈ ਆਈਸੀਐਮਆਰ-ਐਨਆਈਐਮਆਰ, ਹੋਰ ਖੋਜ ਸੰਸਥਾਵਾਂ ਅਤੇ ਨੈਸ਼ਨਲ ਇੰਸਟੀਚਿਊਟ ਆਫ਼ ਇਮਯੂਨੋਲੋਜੀ ਨੇ ਸਾਂਝੇ ਤੌਰ ‘ਤੇ ਪ੍ਰੀ-ਕਲੀਨਿਕਲ ਟ੍ਰਾਇਲ ਕੀਤੇ, ਜਿਸਨੇ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਨਤੀਜੇ ਦਿਖਾਏ।
ਪ੍ਰੀ-ਕਲੀਨਿਕਲ ਡੇਟਾ ਮੁਤਾਬਕ ਇਹ ਟੀਕਾ ਮੌਜੂਦਾ ਸਿੰਗਲ-ਸਟੇਜ ਟੀਕਿਆਂ ਨਾਲੋਂ ਬਿਹਤਰ ਹੈ। ਇਹ ਸਰੀਰ ਦੀ ਲੰਬੇ ਸਮੇਂ ਦੀ ਇਮਿਊਨਿਟੀ ਨੂੰ ਵਧਾਉਂਦਾ ਹੈ ਅਤੇ ਕਮਰੇ ਦੇ ਤਾਪਮਾਨ ‘ਤੇ 9 ਮਹੀਨਿਆਂ ਤਕ ਸਥਿਰ ਰਹਿ ਸਕਦਾ ਹੈ। ਭਾਰਤ ਵਿਚ ਮਲੇਰੀਆ ਨਾਲ ਲੜਨ ਦੇ ਯਤਨ ਕਈ ਸਾਲਾਂ ਤੋਂ ਚੱਲ ਰਹੇ ਹਨ। 2015 ਅਤੇ 2023 ਦੇ ਵਿਚਕਾਰ ਮਲੇਰੀਆ ਦੇ ਮਾਮਲਿਆਂ ਵਿਚ 80.5% ਦੀ ਕਮੀ ਆਈ ਹੈ ਅਤੇ ਮੌਤਾਂ ਵਿਚ 78.38% ਦੀ ਗਿਰਾਵਟ ਆਈ ਹੈ। ਇਸ ਤਰੰਕੀ ਕਾਰਨ ਭਾਰਤ ਹੁਣ ਡਬਲਿਊਐਚਓ ਦੇ ‘ਹਾਈ ਬਰਡਨ ਟੂ ਹਾਈ ਇਮਪੈਕਟ’ (ਐਚਬੀਐਚਆਈ) ਸਮੂਹ ਤੋਂ ਬਾਹਰ ਆ ਗਿਆ ਹੈ। ਸਰਕਾਰ ਦਾ ਟੀਚਾ 2027 ਤਕ ਮਲੇਰੀਆ ਦੇ ਮਾਮਲਿਆਂ ਨੂੰ ਜ਼ੀਰੋ ਤਕ ਘਟਾਉਣਾ ਅਤੇ 2030 ਤਕ ਬਿਮਾਰੀ ਦਾ ਪੂਰੀ ਤਰ੍ਹਾਂ ਖਾਤਮਾ ਕਰਨਾ ਹੈ। ਦੱਸਣਯੋਗ ਹੈ ਕਿ ਵਿਸ਼ਵ ਪੱਧਰ ‘ਤੇ ਮਲੇਰੀਆ ਹਰ ਸਾਲ ਲਗਭਗ 263 ਮਿਲੀਅਨ ਲੋਕਾਂ ਨੂੰ ਪ੍ਰਭਾਵਿਤ ਕਰਦਾ ਹੈ ਅਤੇ 6 ਲੱਖ ਤੋਂ ਵੱਧ ਲੋਕਾਂ ਦੀ ਮੌਤ ਹੋ ਜਾਂਦੀ ਹੈ। ਅਜਿਹੀ ਸਥਿਤੀ ਵਿਚ ਭਾਰਤ ਦੁਆਰਾ ਦੇਸੀ ਟੀਕੇ ਦੀ ਖੋਜ ਨੂੰ ਨਾ ਸਿਰਫ਼ ਦੇਸ਼ ਲਈ ਸਗੋਂ ਵਿਸ਼ਵ ਸਿਹਤ ਦੇ ਮਾਮਲੇ ਵਿਚ ਵੀ ਇਕ ਵੱਡੀ ਪ੍ਰਾਪਤੀ ਮੰਨਿਆ ਜਾ ਰਿਹਾ ਹੈ।